糖尿病神经病变(专业版)
糖尿病神经病变是一种与糖尿病有关的神经损伤。它会造成脚、腿和眼睛等损害,也对控制内脏的自主神经如消化、血压和心脏等形成损伤。
其他名称:糖尿病神经损伤
英文名称:Diabetic Neuropathy,Nerve Damage of Diabetes
糖尿病神经病变是最主要的糖尿病并发症之一,常见类型如下:
值得注意的是,糖尿病神经病变在糖尿病前期就已经存在了。
综合选项可包括如下:
调整饮食与生活方式
防控糖尿病神经病变,首先是稳定血糖水平,具体可参照2型糖尿病管理有关内容如:
营养与草本综合干预
以下是基于循证医学和营养学有关文献综合的结果。
有助于防控糖尿病神经病变的营养和草本,主要包括如下:
血糖升高通过多种机制导致糖尿病并发症,包括神经病变。例如:高糖会促进炎症和糖化,并干扰神经元的血流,所有这些都会导致神经病变。不幸的是,大多数常规药物治疗旨在缓解症状,而没有针对潜在的机制1。不过,研究表明,一些自然干预措施可以调节神经病变发展的生物学途径。因此,通过采取措施将空腹血糖水平保持在最佳范围内,并补充天然化合物来减轻过量葡萄糖的负面影响,以确保防止糖尿病并发症。关于如何控制血糖水平,可参阅本网站专文:2型糖尿病 >>。
以下自然干预措施有助于管理糖尿病神经病变、防止并发症产生:
1.硫辛酸:
一种在体内产生、可发挥多种有益作用的化合物,尤其是在葡萄糖代谢方面1。事实上,硫辛酸在德国已被批准用于治疗糖尿病神经病变1,2。此外,硫辛酸可能对糖尿病患者的葡萄糖代谢产生积极影响3。硫辛酸帮助对抗糖尿病神经病变的重要机制包括抑制糖化和炎症4,5。据报道,硫辛酸可以在神经元细胞培养中防止氧化损伤6。(Bharat 2002)它还改善了神经的血液流动,使它们能够更有效地利用能量7,1。
一项临床试验表明,在3周内每天3次服用600mg的α-硫辛酸,可显著改善12名糖尿病神经病变患者的症状。在另一项试验中,181名患者被分为每天接受安慰剂或600、1200或1800mg α-硫辛酸组。1800mg/天组在短短一周内症状显著改善,600mg和1200mg组在第2周时症状有所改善1。在这两项试验中,疼痛和灼烧感都得到了缓解。另一项研究发现,在4年的时间里,每天口服600mg硫辛酸可以改善神经性症状,减缓轻度至中度糖尿病神经病变的进展8。
其他试验表明,静脉注射硫辛酸对糖尿病神经病变也有益。一项研究表明,每天静脉注射α-硫辛酸3周是治疗糖尿病神经病变的有效方法,另一项试验报告称,静脉注射2-4周是有效的1,9。
注意:硫辛酸有二种形式的补充剂:α-硫辛酸和R-硫辛酸。有证据表明,R-硫辛酸的钠盐比a-硫辛酸更具生物利用性10。
2.乙酰L肉碱(ALC)和L肉碱:
肉碱是一种对线粒体能量产生很重要的氨基酸类化合物。对肉碱在糖尿病神经病变中的作用源于有证据表明,患有并发症(包括糖尿病神经病变)的糖尿病患者的血清和总肉碱水平低于没有并发症的糖尿病患者11。因此,ALC和L-肉碱均已被研究为糖尿病神经病变的潜在治疗方法。补充肉碱可能有助于对抗肉碱缺乏症,改善胰岛素抵抗,使细胞更有效地利用葡萄糖,帮助受损神经纤维再生,或支持受损神经元更有效地运输细胞内成分11。
已经对补充肉碱对糖尿病神经病变的影响进行了多项人体试验。一项研究发现,L-肉碱(每天2g,持续10个月)可以改善神经传导速度,而神经传导速度在糖尿病神经病变中受损12。对ALC的研究发现,它减轻了糖尿病神经病变患者的疼痛,改善了腿部的振动感,并增加了神经再生13-15。补充肉碱也可能有助于治疗糖尿病引起的自主神经病变,对动物模型进行的一项研究发现ALC降低了糖尿病自主神经病变的心血管体征16。
3.十六酰胺乙醇(PEA):
一种天然存在于全身组织中的脂质化合物,包括中枢神经系统。在大豆卵磷脂、蛋黄和花生等食物中也存在17。越来越多的研究表明,补充PEA可能有效缓解各种原因引起的疼痛,而不会引发不良副作用18,19。大多数现有的临床前研究表明,PEA通过改变某些基因的表达和减少炎症信号传导发挥作用,但也提出了其镇痛作用的其他可能机制,包括其通过神经系统中的大麻素受体刺激信号传导的能力20,21。
几项临床试验表明,PEA可以减轻多种原因引起的疼痛,包括糖尿病神经病变、化疗诱导的周围神经病变、坐骨神经压迫、腕管综合征、骨关节炎、腰痛、背部手术失败、中风相关神经痛、多发性硬化症、牙痛、慢性骨盆疼痛、疱疹后神经痛和阴道疼痛等22。在一项针对因各种情况而无法通过常规治疗控制疼痛的慢性疼痛患者的观察性研究中,在三周内每天二次添加600mg PEA,然后在四周内每天一次,降低了所有完成研究的参与者的平均疼痛强度得分23。。
在一项随机对照试验中,636名因坐骨神经压迫而疼痛的参与者接受了每天300mg PEA、每天600mg PEA或安慰剂以及他们常用的止痛药,为期三周。两种剂量的PEA都比安慰剂更能减轻疼痛,而且高剂量比低剂量更有效。事实上,600mg组的疼痛评分降低了50%以上24。在118名神经疼痛患者中,30天的标准治疗加上每天600mg PEA比单独的标准治疗更有效25。一项随机临床试验发现,在缓解颞下颌关节(TMJ)疼痛方面,一周内每天900mg PEA,一周后每天600mg PEA比布洛芬更有效,布洛芬的剂量为600mg,两周内每天三次26。
对PEA的微粉化制剂也进行了研究。微粉化会产生更小的颗粒,这些颗粒可能更容易被吸收。剂量为600–1200mg/天的微粉化PEA可减轻糖尿病或创伤相关神经疼痛、背部手术失败后的慢性疼痛和拔牙后的急性疼痛受试者的疼痛27-29。在一份关于100例与脊柱疾病相关的神经疼痛的报告中,将超微粉化PEA补充剂纳入疼痛管理治疗显示出了有希望的结果30。一项荟萃分析发现,患有子宫内膜异位症引起的慢性盆腔疼痛的女性似乎受益于每天800mg微粉化PEA加上每天80mg虎杖苷(Polydatin)的组合,虎杖苷是一种在葡萄和红酒中发现的天然自由基减少剂31。在一项随机对照试验中,PEA和虎杖苷的组合在减轻肠易激综合征患者腹痛方面比安慰剂更有效32。
4. N-乙酰半胱氨酸(NAC):
既是体内谷胱甘肽合成前体,NAC本身也是一种抗氧化剂。它可以保护神经元免受氧化损伤33。此外,NAC已被证明可以抑制糖基化终产物(AGEs)的形成34。对糖尿病神经病变动物模型的多项研究发现,NAC可以防止神经元死亡并防止神经损伤33,2。
5.维生素B族:
B族维生素是一种维生素家族,在人体中发挥着许多作用,尤其是在细胞能量生成和神经系统功能中35。
5.1.维生素B1(硫胺素)和苯磷硫胺:
硫胺素缺乏可直接导致神经病变2。先前研究发现硫胺素可以用于治疗疼痛的糖尿病神经病变。苯磷硫胺是硫胺素的脂溶性衍生物,更容易被消化道吸收36。
苯磷硫胺可能调节导致糖尿病神经病变的几种途径:AGEs的形成、蛋白激酶C途径,以及由于高糖水平可能在细胞内发生的损伤性变化37,38。它也可能有助于预防导致神经病变的血管问题39。(Stracke 2008)多项临床试验已经检验了苯磷硫胺对糖尿病神经病变的影响39,40,2,并发现特别是在每天300至600mg的剂量下,它能够缓解糖尿病神经病变症状,尤其是疼痛。
5.2.维生素B12:它对神经系统的功能至关重要,缺乏B12会导致严重的周围神经病变2。此外,糖尿病神经病变患者通常具有高水平的破坏血管的化合物—同型半胱氨酸,在维生素B12水平较低的情况下,同型半胱氨酸会升高41。还研究了补充维生素B12治疗糖尿病神经病变的潜在益处,维生素B12的活性形式—甲钴胺,它对神经组织具有亲和力,在这方面已经得到了广泛的研究42。对糖尿病神经病变动物模型的研究发现,甲钴胺可以减轻糖尿病神经病变引起的损害,可能通过调节蛋白激酶C信号通路或激活化学信号来帮助神经存活和再生42,43。
在多项临床试验中发现,2mg甲钴胺、3mg L-甲基叶酸和35mg 5’-磷酸吡哆醛(维生素B6形式之一)的组合可以改善神经病变症状,并有助于维持下肢小神经的健康44-46。这三种营养素的组合也被发现有助于降低糖尿病神经病变患者的住院和医疗费用47。对甲钴胺的单独研究也令人鼓舞,口服甲基钴胺(每天1500mcg)和注射甲基钴胺(每天2000mcg)均可改善麻木、反射、对振动的敏感性、针刺刺激、步态和疼痛48,49。一项研究甚至发现,甲钴胺比常用于治疗糖尿病神经性疼痛的抗抑郁药去甲替林更有效48。
5.3.叶酸和维生素B6:与甲钴胺一样,维生素B6对神经功能很重要,而叶酸可能有助于改善供应神经的血管功能45。如前所述,叶酸和维生素B6衍生物以及甲钴胺已在临床试验中进行了测试,并显示出阳性结果44-46。
6. 维生素C和E:
研究发现,糖尿病患者的维生素C水平较低;这似乎是疾病本身的结果,而不是维生素C的饮食摄入减少50。另一项表明维生素C重要性的证据是,患有糖尿病神经病变的人体内“还原”的维生素C水平升高,而维生素C已经被人体使用。这表明糖尿病神经病变给身体储存的维生素C带来了额外的压力。研究表明,糖尿病神经病变患者和糖尿病动物的维生素E水平也有所下降51。已经发现,单独补充维生素E可以改善周围神经病变的症状52,还可以改善2型糖尿病患者的神经传导53。此外,包括维生素C和E等微量元素的治疗在一项临床试验中表明都是有益的54。
7.矿物质:
一项研究发现,糖尿病患者的头发和血液中锌、铬和锰含量较低,这表明这些营养素的缺乏可能与糖尿病神经病变有关55。此外,糖尿病是导致继发性镁缺乏的最常见疾病,25-30%的1型糖尿病患者和13.5-47.7%的2型糖尿病患者存在镁缺乏症56。在糖尿病大鼠模型中,口服镁或镁释放化合物有助于保护神经免受糖尿病神经病变的影响56,57。
一项临床试验还发现,连续5年每天口服500mg镁补充剂可以减缓人类糖尿病神经病变的进展58。锌也显示出治疗糖尿病神经病变的前景。临床研究发现,补充锌有助于改善血糖控制,还可以降低糖尿病神经病变的严重程度59,60。最后,一项临床研究发现,连续4个月补充微量营养素,包括锌和镁,以及维生素C和E,无论是否补充B组的维生素,都能改善糖尿病神经病变的症状54。
8.欧米伽-3脂肪酸:
历来被研究其对血管疾病的影响,因为高ω-3脂肪酸的饮食与较低的心脏病风险有关。虽然缺乏关于ω-3脂肪酸特别是在糖尿病神经病变中的益处的临床试验数据,但糖尿病神经病变的几种动物模型表明了这些重要脂肪的潜在作用61。一种理论认为,糖尿病神经病变与受影响神经膜中ω-3脂肪酸水平较低有关。对糖尿病神经病变动物模型的两项不同研究发现,补充ω-3脂肪酸可以改善糖尿病神经病变的症状62,63。
9.维生素D:
据报道,维生素D缺乏是糖尿病周围神经病变发展的独立风险因素64,补充维生素D可能有助一些患有神经病变的糖尿病患者。维生素D缺乏症同时存在于1型和2型糖尿病患者中,在有明显神经病变症状和疼痛阈值降低的糖尿病患者中更为常见65。一项针对患有糖尿病的成年人的研究报告称,维生素D不足(定义为水平低于30ng/mL)与更严重的自我报告的糖尿病神经病变症状有关,即使对几个变量进行了调整,如肥胖或糖尿病持续时间和控制,这种关联仍然存在66。
关于补充维生素D对糖尿病神经病变和维生素D缺乏症患者的影响,已经发表了两篇不同的论文。一项针对51名2型糖尿病患者的研究发现,补充维生素D可将报告的疼痛水平降低近50%,并表明维生素D可作为糖尿病神经病变引起的疼痛患者的“止痛药”67。第二个是一名维生素D缺乏症和糖尿病神经病变患者的病例报告,该患者严重到需要使用麻醉性止痛药来控制症状。该患者通过补充维生素D获得了显著的疼痛缓解,这表明服用维生素D可以显著缓解糖尿病神经病变症状65。
维生素D不足在各类人群中较为普遍,一般维持健康的血清25-羟基维生素D水平范围:50-80ng/mL。
10.植物化学素:
10.1.姜黄素:
姜黄素阿育吠陀医学的重要药草姜黄的主要活性成分。姜黄素具有抗氧化、抗炎特性。有证据表明,姜黄素可以通过降低氧化氮的自由基水平和抑制炎症介质TNF-α来调节疼痛感觉68。因此,它可能会干扰糖尿病神经病变损伤神经的疼痛信号,并防止对神经的氧化损伤69。
姜黄素用于糖尿病神经病变的主要证据来源于临床前研究。在糖尿病神经病变的动物模型中,已发现姜黄素可减少中枢和外周神经系统神经的氧化损伤,并减少了细胞死亡69,70。其他研究发现,姜黄素在这种疾病的动物模型中降低了炎症和对疼痛的敏感性71-73。
10.2.白藜芦醇和葡萄籽提取物:
白藜芦醇是一种天然的植物化学物质,存在于葡萄、红酒和日本虎杖中。在糖尿病动物模型中,白藜芦醇由于其抑制炎症以及减少氧化应激和DNA损伤的能力而被证明可以预防神经病变74,75。在另一项临床前研究中,发现白藜芦醇与胰岛素联合使用可降低对疼痛的敏感性71。
葡萄籽原花青素在糖尿病动物模型中被证明可以提高运动神经的传导速度并调节疼痛感;它们还减少了神经周围被称为髓鞘的保护鞘的损失。此外,它们减少了AGEs的产生,这表明它们还减少了糖尿病神经病变对神经的氧化损伤76
更多内容可点击其个性化综合干预方案如下:
以及参阅本如下专文的相关内容:
医疗干预
医学上,仍然没有针对糖尿病神经病变的预防治疗措施,只能对症治疗。
取决于病程发展的症状。药物可用于缓解疼痛、灼烧感、刺痛或麻木等。治疗这些症状的药物与用于治疗癫痫发作和抑郁症的基本相同。
治疗疼痛的另一个选择称为经皮神经电刺激(TENS),将无痛的电信号通过皮肤发送到神经。医生可能会提供这种治疗。
手术治疗:(略)
自我护理
足部护理:对于糖尿病神经病变,需要特别关注脚部健康,因为足部神经是最常受神经病变影响的神经。脚部护理包括定期拜访医生,仔细检查、清洁和处理伤口等。此外,一定要穿合脚的鞋子,注意腿脚保暖,维持血液循环。
参考文献:
1. McIlduff CE et al. Critical Appraisal of the Use of Alpha Lipoic Acid (Thiooctic Acid) in the Treatment of Symptomatic Diabetic Polyneuropathy. Therapeutics and Clinical Risk Management, 2011; 7: 377-385.
2. Head KA. Peripheral Neuropathy: Pathogenic Mechanisms and Alternative Therapies. Alternative Medicine Review, 2006; 11(4): 294-329.
3. Korotchkina LG et al. R-lipoic acid inhibits mammalian pyruvate dehydrogenase kinase. Free radical research. Oct 2004;38(10):1083-1092.
4. Thirunavukkarasu V et al. Lipoic acid improves glucose utilisation and prevents protein glycation and AGE formation. Die Pharmazie. Oct 2005;60(10):772-775.
5. Kunt T et al. Alpha-lipoic acid reduces expression of vascular cell adhesion molecule-1 and endothelial adhesion of human monocytes after stimulation with advanced glycation end products. Clinical science. Jan 1999;96(1):75-82.
6. Bharat S et al. Pre-treatment with R-lipoic acid alleviates the effects of GSH depletion in PC12 cells: implications for Parkinson's disease therapy. Neurotoxicology. Oct 2002;23(4-5):479-486.
7. Bertolotto F et al. Combination of Alpha Lipoic Acid and Superoxide Dismutase Leads to Physiological and Symptomatic Improvements in Diabetic Neuropathy. Drugs Research and Development, 2012; 12(1): 29-34.
8. Ziegler D et al. Efficacy and Safety of Antioxidant Treatment with Alpha-Lipoic Acid Over 4 Years in Diabetic Polyneuropathy. Diabetes Care, 2011; 34: 2054-2060.
9. Han T et al. A Systematic Review and Meta-Analysis of Alpha-Lipoic Acid in the Treatment of Diabetic Peripheral Neuropathy. European Journal of Endocrinology, 2012; 167: 465-471.
10. Carlson DA et al. The plasma pharmacokinetics of R-(+)-lipoic acid administered as sodium R-(+)-lipoate to healthy human subjects. Alternative medicine review. Dec 2007;12(4):343-351.
11. Evans JD et al. Role of Acetyl-L-Carnitine in the Treatment of Diabetic Peripheral Neuropathy. Annals of Pharmacotherapy, 2008; 42: 1686-1691.
12. Ulvi H et al. Effect of L_Carnitine on Diabetic Neuropathy and Ventricular Dispersion in Patients with Diabetes Mellitus. Turkish Journal of Medical Science, 2010; 40(2): 169-175.
13. Bansal V et al. Diabetic Neuropathy. Postgraduate Medical Journal, 2006; 82: 95-100.
14. Sima AAF et al. Acetyl-L-Carnitine Improves Pain, Nerve Regeneration, and Vibratory Perception in Patients with Chronic Diabetic Neuropathy. Diabetes Care, 2005; 28(1): 89-94.
15. Adriaensen H et al. Critical Review of Oral Drug Treatments for Diabetic Neuropathic Pain – Clinical Outcomes Based on Efficacy and Safety Data from Placebo-Controlled and Direct Comparative Studies. Diabetes/Metabolism Research and Reviews, 2005; 21: 231-240.
16. Giudice PL et al. Autonomic Neuropathy in Streptozotocin Diabetic Rats: Effect of Acetyl-L-Carnitine. Diabetes Research and Clinical Practice, 2002; 56: 173-180.
17. Mattace Raso G et al. Palmitoylethanolamide in CNS health and disease. Pharmacological Research. Aug 2014;86:32-41.
18. Artukoglu BB et al. Efficacy of Palmitoylethanolamide for Pain: A Meta-Analysis. Pain Physician. Jul 2017;20(5):353-362.
19. Paladini A et al. Palmitoylethanolamide, a Special Food for Medical Purposes, in the Treatment of Chronic Pain: A Pooled Data Meta-analysis. Pain Physician. Feb 2016;19(2):11-24.
20. Gabrielsson L et al. Palmitoylethanolamide for the treatment of pain: pharmacokinetics, safety and efficacy. British Journal of Clinical Pharmacology. Oct 2016;82(4):932-942.
21. Khasabova IA et al. Peroxisome proliferator-activated receptor alpha mediates acute effects of palmitoylethanolamide on sensory neurons. The Journal of Neuroscience. Sep 12 2012;32(37):12735-12743.
22. Keppel Hesselink JM et al. Therapeutic utility of palmitoylethanolamide in the treatment of neuropathic pain associated with various pathological conditions: a case series. Journal of Pain Research. 2012;5:437-442.
23. Gatti A et al. Palmitoylethanolamide in the treatment of chronic pain caused by different etiopathogenesis. Pain Medicine (Malden, Mass.). Sep 2012;13(9):1121-1130.
24. Keppel Hesselink JM et al. Palmitoylethanolamide, a neutraceutical, in nerve compression syndromes: efficacy and safety in sciatic pain and carpal tunnel syndrome. Journal of Pain Research. 2015;8:729-734.
25. Dominguez CM et al. N-palmitoylethanolamide in the treatment of neuropathic pain associated with lumbosciatica. Pain Management. Mar 2012;2(2):119-124.
26. Marini I et al. Palmitoylethanolamide versus a nonsteroidal anti-inflammatory drug in the treatment of temporomandibular joint inflammatory pain. Journal of Orofacial Pain. Spring 2012;26(2):99-104.
27. Cocito D et al. Short-term efficacy of ultramicronized palmitoylethanolamide in peripheral neuropathic pain. Pain Research and Treatment. 2014;2014:854560.
28. Paladini A et al. Palmitoylethanolamide in the Treatment of Failed Back Surgery Syndrome. Pain Research and Treatment. 2017;2017:1486010.
29. Bacci C et al. Randomized split-mouth study on postoperative effects of palmitoylethanolamide for impacted lower third molar surgery. ISRN Surgery. 2011;2011:917350.
30. Chirchiglia D et al. Nonsurgical lumbar radiculopathies treated with ultramicronized palmitoylethanolamide (umPEA): A series of 100 cases. Neurol Neurochir Pol. 2018 Jan-Feb;52(1):44-47.
31. Indraccolo U et al. Micronized palmitoylethanolamide/trans-polydatin treatment of endometriosis-related pain: a meta-analysis. Annali Dell'Istituto Superiore di Sanita. Apr-Jun 2017;53(2):125-134.
32. Cremon C et al. Randomised clinical trial: the analgesic properties of dietary supplementation with palmitoylethanolamide and polydatin in irritable bowel syndrome. Alimentary Pharmacology & Therapeutics. Apr 2017;45(7):909-922.
33. Kamboj SS et al. N-Acetylcysteine Inhibits Hyperglycemia-Induced Oxidative Stress and Apoptosis Markers in Diabetic Neuropathy. Journal of Neurochemistry, 2010; 112: 77-91.
34. Nakayama M et al. Suppression of N(epsilon)-(carboxymethyl)lysine generation by the antioxidant N-acetylcysteine. Peritoneal dialysis international. May-Jun 1999;19(3):207-210.
35. Selhub J et al. B vitamins, homocysteine, and neurocognitive function in the elderly. The American journal of clinical nutrition. Feb 2000;71(2):614s-620s.
36. Sanchez-Ramirez GM et al. Benfotiamine Relieves Inflammatory and Neuropathic Pain in rats. European Journal of Pharmacology, 2006; 530: 48-53.
37. Varkonyi T et al. Diabetic Neuropathy: New Strategies for Treatment. Diabetes, Obesity and Metabolism, 2008; 10: 99-108.
38. Balakumar P et al. The Multifaceted Therapeutic Potential of Benfotiamine. Pharmacological Research, 2010; 61: 482-488.
39. Stracke H et al. Benfotiamine in Diabetic Polyneuropathy (BENDIP): Results of a Randomised, Double Blind, Placebo-Controlled Clinical Study. Exp Clin Endocrinol Diabetes. 2008 Nov;116(10):600-5.
40. Haupt E et al. Benfotamine in the treatment of diabetic polyneuropathy—a three-week randomized, controlled pilot study (BEDIP study). Int J Clin Pharmacol Ther. 2005;43(2):71-77.
41. Fahmy E et al. Estimation of Serum Homocysteine Level in Patients with Type 2 Diabetic Neuropathy. Egyptian Journal of Neurology Psychiatry and Neurosurgery, 2010; 47(1): 59-66.
42. Mizukami H et al. Methylcobalamin Effects of Diabetic Neuropathy and Nerve Protein Kinase C in Rats. European Journal of Clinical Investigation, 2011; 41(4): 442-450.
43. Okada K et al. Methylcobalamin Increases Erk1/2 and Akt Activities through the Methylation Cycle and Promotes Nerve Regeneration in a Rat Sciatic Nerve Injury Model. Experimental Neurology, 2010;222: 191-203.
44. Jacobs AM et al. Management of Diabetic Small-Fiber neuropathy with Combination L-Methylfolate, Methylcobalamin, and Pyridocal 5’-Phosphate. Reviews of Neurological Diseases, 2011; 8(1/2): 1-9.
45. Fonseca VA et al. Metanx in Type 2 Diabetes with Peripheral Neuropathy: A Randomized Trial. The American Journal of Medicine (2013) 126, 141-149.
46. Walker MJ et al. Improvement of Cutaneous Sensitivity in Diabetic Peripheral Neuropathy with Combination L-Methylfolate, Methylcobalamin, and Pyridoxal 5’Phosphate. Reviews in Neurological Diseases, 2010; 7(4): 132-139.
47. Wade RL et al. Impact of L-Methylfolate Combination therapy Among Diabetic Peripheral Neuropathy Patients. American Journal of Pharmacological Benefits, 2012; 4(5): 218-225.
48. Talaei A et al. Vitamin B12 may be more effective than nortriptyline in improving painful diabetic neuropathy. International Journal of Food Sciences and Nutrition, 2009;60 Suppl 5:71-6.
49. Dominguez JC et al. A prospective, open label, 24-week trial of methylcobalamin in the treatment of diabetic polyneuropathy. Journal of Diabetes Mellitus, 2012; 2(4): 408-412.
50. Sinclair AJ et al. Low Plasma Ascorbate Levels in Patients with Type 2 Diabetes Mellitus Consuming Adequate Dietary Vitamin C. Diabetic Medicine, 1994; 11(9): 893-898.
51. Ziegler D et al. Oxidative Stress and Antioxidant Defense in Relation to the Severity of Diabetic Polyneuropathy and Cardiovascular Autonomic Neuropathy. Diabetes Care, 2004; 27: 2178-2183.
52. Martinello F et al. Supplemental therapy in isolated vitamin E deficiency improves the peripheral neuropathy and prevents the progression of ataxia. Journal of Neurological Sciences 156 (1998) 177–179.
53. Tutuncu NB et al. Reversal of defective nerve conduction with vitamin E supplementation in type 2 diabetes: a preliminary study. Diabetes Care. 1998 Nov;21(11):1915-8.
54. Farvid MS et al. Improving neuropathy scores in type 2 diabetic patients using micronutrients supplementation. Diabetes Research and Clinical Practice, 2011; 93: 86-94.
55. Gul Kazi T et al. Copper, Chromium, Manganese, Iron, Nickel, and Zinc Levels in Biological Samples of Diabetes Mellitus Patients. Biol Trace Elem Res (2008) 122:1–18
56. Rondon LJ et al. Magnesium attenuates chronic hypersensitivity and spinal cord NMDA receptor phosphorylation in a rat model of diabetic neuropathic pain. Journal of Physiology, 2010; 588(21): 4205-4215.
57. Hosseini A et al. Benefit of magnesium-25 carrying porphyrinfullerenenanoparticles in experimental diabetic neuropathy. International Journal of Nanomedicine 2010:5 517–523.
58. De Leeuw I et al. Long term magnesium supplementation influences favourably the natural evolution of neuropathy in Mg-depleted type 1 diabetic patients (T1dm). Magnesium Research. 2004;17(2):109-114.
59. Jayawardena R et al. Effects of zinc supplementation on diabetes mellitus: a systematic review and meta-analysis. Diabetology & Metabolic Syndrome 2012, 4:13
60. Hayee MA et al. Diabetic Neuropathy and Zinc Therapy. Bangladesh Medical Reseanch Council Bull, 2005; 31(2): 62-67.
61. De Caterina R et al. n-3 Fatty Acids in the Treatment of Diabetic Patients. Diabetes Care, 2007l 30(4): 1012-1026.
62. Gerbi A et al. Fish Oil Supplementation Prevents Diabetes-Induced Nerve Conduction Velocity and Neuroanatomical Changes in Rats. The Journal of Nutrition, 1999; 129: 207-213.
63. Coste TC et al. Neuroprotective Effect of Docosahexaenoic Acid–Enriched Phospholipids in Experimental Diabetic Neuropathy. Diabetes, 2003; 52: 2578-2585.
64. Shehab D et al. Does Vitamin D deficiency play a role in peripheral neuropathy in Type 2 diabetes? Diabetic Medicine, 2012;29(1):43-9.
65. Bell DSH. Reversal of the Symptoms of Diabetic Neuropathy through Correction of Vitamin D Deficiency in a Type 1 Diabetic Patient. Case Rep Endocrinol. 2012;2012:165056.
66. Soderstrom LH et al. Association between vitamin D and diabetic neuropathy in a nationally representative sample: results from 2001-2004 NHANES. Diabetic Medicine, 2012;29(1):50-5.
67. Lee P et al. Vitamin D as an Analgesic for Patients With Type 2 Diabetes and Neuropathic Pain. Archives of Internal Medicine, 2008; 168(7): 771-772.
68. Sharma S et al. Curcumin attenuates thermal hyperalgesia in a diabetic mouse model of neuropathic pain. European Journal of Pharmacology, 2006; 536: 256-261.
69. Lakshmanan AP et al. Curcumin attenuates hyperglycaemia-mediated AMPK activation and oxidative stress in cerebrum of streptozotocin-induced diabetic rat. Free Radical Research, July 2011; 45(7): 788–795.
70. Acar A et al. Oxidative Damage is Ameliorated by Curcumin Treatment in Brain and Sciatic Nerve of Diabetic Rats. International Journal of Neuroscience, 2012; 122(7): 367-372.
71. Sharma S et al. Effect of Insulin and its Combination with Resveratrol or Curcumin in Attenuation of Diabetic Neuropathic Pain: Participation of Nitric Oxide and TNF-alpha. Phytotherapy Research, 2007; 21: 278-283.
72. Kulkarni SK et al. An Overview of Curcumin in Neurological Disorders. Indian J Pharm Sci. 2010 Mar-Apr; 72(2): 149–154.
73. Attia HN et al. Protective effects of combined therapy of gliclazide with curcumin in experimental diabetic neuropathy in rats. Behavioural Pharmacology, 2012; 23(2): 153-161.
74. Kumar A et al. Effects of resveratrol on nerve functions, oxidative stress and DNA fragmentation in experimental diabetic neuropathy. Life Sciences, 2007;80(13):1236-44.
75. Kumar A et al. NF-kappaB inhibitory action of resveratrol: a probable mechanism of neuroprotection in experimental diabetic neuropathy. Biochemical and Biophysical Research Communications 2010;394(2):360-5.
76. Cui XP et al. Effects of grape seed proanthocyanidin extracts on peripheral nerves in streptozocin-induced diabetic rats. Journal of Nutritional Science and Vitaminology (Tokyo), 2008;54(4):321-8.
美国糖尿病协会
http://www.diabetes.org
美国国立卫生研究院糖尿病、消化和肾病研究所
https://www.niddk.nih.gov
加拿大糖尿病协会
http://www.diabetes.ca
加拿大卫生部
http://www.hc-sc.gc.ca
免责声明和安全信息
英文名称:Diabetic Neuropathy,Nerve Damage of Diabetes
定义
糖尿病神经病变是一种与糖尿病有关的神经损伤。它会造成脚、腿和眼睛等损害,也对控制内脏的自主神经如消化、血压和心脏等形成损伤。糖尿病神经病变是最主要的糖尿病并发症之一,常见类型如下:
- 周围神经病变:最常见形式,影响感觉神经、导致疼痛或缺乏感觉。首先是手和脚,其次是腿和手臂。
- 自主神经病变:涉及消化、心率、血压控制和出汗等内脏器官的自主神经。
- 近端神经病变:也称为腰骶部放射综合征神经痛,或糖尿病性肌萎缩症,影响下半身如臀部、大腿等,并可导致疼痛和虚弱、萎缩等。
- 局灶性神经病和单神经病影响特定神经,导致该神经提供的区域虚弱和/或疼痛,或影响神经的特征性体征和症状。
值得注意的是,糖尿病神经病变在糖尿病前期就已经存在了。
病因
糖尿病神经病变可能由多种因素引起的,包括:- 代谢综合征:血压、胆固醇和血糖异常升高,并造成中心性肥胖。
- 血管损伤
- 自体免疫因素
- 基因因素
- 糖基化:长期的高血糖导致葡萄糖与蛋白质、脂肪等结合产生糖基化,并形成糖基化终产物(AGEs)分布于体内,对神经、血管等造成不可逆的损害。糖基化对神经的损伤通过两种不同的机制发生。首先,神经蛋白的糖基化抑制了它们的功能,这直接影响了神经活动。其次,AGEs可以与神经细胞表面结合,引发炎症反应,进一步损伤神经元
- 低度炎症:炎症在糖尿病神经病变中也起着关键作用。因长期高血糖和AGEs存在可导致多种炎性因子反应,包括肿瘤坏死因子-α,C-反应蛋白(CRP)等,刺激巨噬细胞包围并攻击、损害神经元。
- 毛细血管功能障碍:高血糖可引起微血管收缩、血流缓慢,导致供氧和营养物减少,结果损伤神经元,并引起肌肉逐渐萎缩。
风险因素
可能增加糖尿病神经病变风险的因素包括:- 20年以上的糖尿病史
- 2型糖尿病
- 高血压
- 肥胖
- 缺乏运动锻炼
- 外周动脉疾病
- 高胆固醇
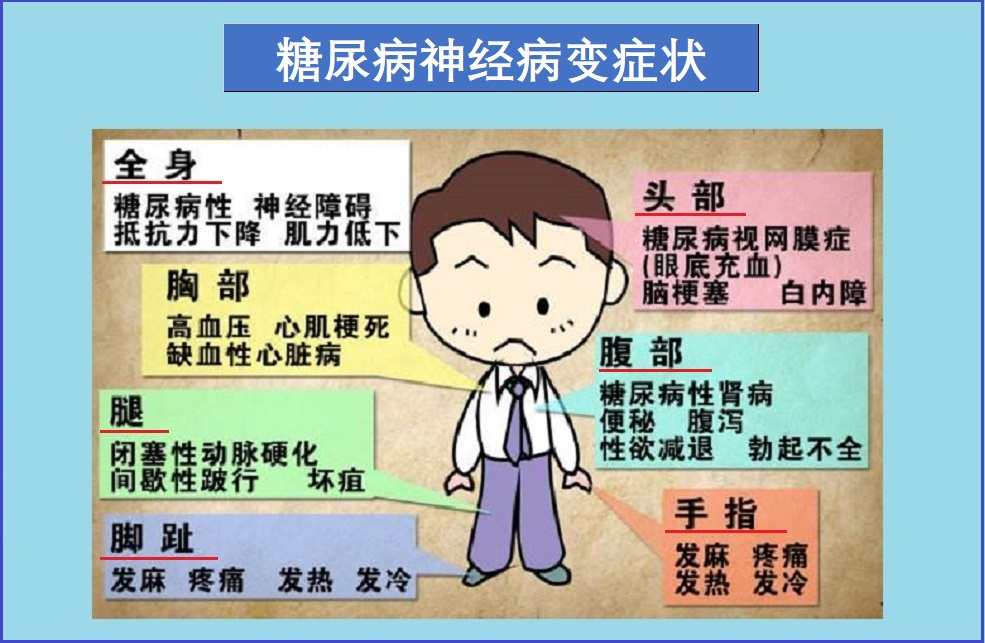
症状
糖尿病神经病变的症状分类如下:- 周围神经病:糖尿病性神经病最常见的类型。它首先影响脚和腿,然后是手和手臂。周围神经病变的体征和症状在夜间通常较差,可能包括:
- 麻木,或感觉疼痛或对温度变化敏感性降低
- 刺痛或烧灼感
- 剧痛或痉挛
- 增加对触摸的敏感度,对于某些人来说,即使床单的重量也会造成痛苦
- 肌肉无力
- 反射消失,特别是在脚踝
- 失去平衡和协调
- 严重的足部问题,如溃疡,感染和骨关节疼痛。
- 自主神经病变:自主神经系统控制着心脏、膀胱、胃肠道、性器官和眼睛。糖尿病可能会影响上述任何区域的神经而导致如下症状:
- 膀胱问题,包括尿路感染、尿潴留或尿失禁。
- 便秘或不受控制的腹泻,或者两者兼而有之。
- 男性勃起功能障碍。
- 女性阴道干燥。
- 缓慢胃排空(胃轻瘫),引起恶心、呕吐、腹胀和食欲不振。
- 吞咽困难。
- 增加或减少出汗。
- 控制体温的问题。
- 眼睛对浅到深光线适应方式的变化。
- 休息时心率增加。
- 坐着或站立后,血压急剧下降,可能会导致头晕或头晕目眩。
- 减少性功能反应。
- 根神经丛神经病变:根神经丛(Radiculoplexus)神经病变影响大腿、臀部和腿部的神经。在2型糖尿病患者和老年患者中更常见。该类型也被称为糖尿病性肌萎缩,或近端神经病变。症状通常在身体的一侧,但有时可能扩散到另一侧:
- 臀部、大腿严重疼痛。
- 大腿肌肉最终弱化和萎缩。
- 从坐姿到站起来困难。
- 如果腹部受到影响,则腹部肿胀。
- 体重下降。
- 单神经病变:单神经病变或局灶性神经病变是对面部、身体中部(躯干)或腿部的特定神经的损伤。这在老年患者中最为常见。单神经病经常会突然发作,并可能导致严重的疼痛。但是,它通常不会导致任何长期问题。症状通常在几周或几个月内没有治疗就会消失。具体症状和体征取决于涉及哪部分神经,可能会在以下方面感到痛苦:
- 小腿或脚。
- 腰部或骨盆。
- 大腿前部。
- 胸部或腹部。
- 眼神难以集中
- 双重视野
- 一只眼睛后面疼痛
- 脸部一侧的瘫痪(贝尔麻痹)
并发症
糖尿病性神经病可引起多种严重并发症,包括如下:- 性功能障碍:自主神经病变通常会损害影响性器官的神经。男性可出现勃起功能障碍,女性可能在阴道润滑和性唤醒方面有困难。
- 脚趾、脚或小腿损伤、截肢:神经损伤可使双腿失去感觉。脚痛和割伤可能会悄悄地变得严重感染或变成溃疡。即使是轻微的脚癣也不会愈合,可能会变成溃疡。在严重的情况下,感染可能扩散到骨头,并且溃疡可能导致组织死亡(坏疽)。可能需要截肢,包括脚趾、脚,甚至小腿。
- 尿路感染和尿失禁:如果控制膀胱的神经受损,则可能无法完全排空膀胱。细菌可以累积在膀胱和肾脏中,引起尿路感染。当需要排尿或控制释放尿液的肌肉时,神经损伤也会影响感觉能力,从而导致尿失禁。
- 消化问题:如果神经损伤涉及到消化道,可引起便秘或腹泻,或两者兼而有之。与糖尿病有关的神经损伤可导致胃轻瘫,这种情况下胃排空速度太慢或根本没有。这会干扰消化并严重影响血糖水平和营养。体征和症状包括恶心、呕吐和腹胀。
- 关节损伤:神经损伤会导致关节退化,通常发生在脚的小关节中。症状包括失去感觉和关节肿胀、不稳定,有时还会出现关节畸形。
- 对低血糖症无察觉:低血糖通常会导致摇晃、出汗和心跳加速。但是如果有自主神经病变,可能不会注意到这些警告信号。
- 体位性低血压:控制血流量的神经受损会影响身体调节血压的能力。这可能会导致久坐后站立时压力急剧下降,引起头晕和晕厥。
- 增加或减少出汗:神经损伤会破坏汗腺的运作,并使身体很难适当地控制它的温度。一些患有自主神经病的人出汗过多,特别是在夜间或进食时。极少汗或根本无汗(无汗症)会危及生命。
疗法
尽早采取预防神经病变措施,可有效抑制或延缓终末期糖尿病并发症。综合选项可包括如下:
调整饮食与生活方式
防控糖尿病神经病变,首先是稳定血糖水平,具体可参照2型糖尿病管理有关内容如:
- 限制摄入糖、精制米面等,可食用低血糖指数(GI)食物,如全谷类(粗粮)。
- 多吃蔬菜、水果等富含纤维食物。
- 健康饮食,包括优质蛋白、不饱和脂肪酸(坚果、深海鱼)等。
- 注意热量平衡,避免摄入过多食物。
- 一日三餐均匀,避免血糖水平波动过大。
- 避免高甜度的食物和饮料。
- 经常运动锻炼,可改善胰岛素敏感性:
- 糖尿病初期,坚持每周5天,每天30-60分钟中强度运动。
- 糖尿病中晚期或老年糖尿病,遵循医生指导的合适运动计划。
- 保持健康的体重。
- 良好睡眠,睡眠差可加重血糖不稳。
- 学会和运用压力管理,如按摩、瑜伽、冥想和深呼吸等
营养与草本综合干预
以下是基于循证医学和营养学有关文献综合的结果。
有助于防控糖尿病神经病变的营养和草本,主要包括如下:
血糖升高通过多种机制导致糖尿病并发症,包括神经病变。例如:高糖会促进炎症和糖化,并干扰神经元的血流,所有这些都会导致神经病变。不幸的是,大多数常规药物治疗旨在缓解症状,而没有针对潜在的机制1。不过,研究表明,一些自然干预措施可以调节神经病变发展的生物学途径。因此,通过采取措施将空腹血糖水平保持在最佳范围内,并补充天然化合物来减轻过量葡萄糖的负面影响,以确保防止糖尿病并发症。关于如何控制血糖水平,可参阅本网站专文:2型糖尿病 >>。
以下自然干预措施有助于管理糖尿病神经病变、防止并发症产生:
1.硫辛酸:
一种在体内产生、可发挥多种有益作用的化合物,尤其是在葡萄糖代谢方面1。事实上,硫辛酸在德国已被批准用于治疗糖尿病神经病变1,2。此外,硫辛酸可能对糖尿病患者的葡萄糖代谢产生积极影响3。硫辛酸帮助对抗糖尿病神经病变的重要机制包括抑制糖化和炎症4,5。据报道,硫辛酸可以在神经元细胞培养中防止氧化损伤6。(Bharat 2002)它还改善了神经的血液流动,使它们能够更有效地利用能量7,1。
一项临床试验表明,在3周内每天3次服用600mg的α-硫辛酸,可显著改善12名糖尿病神经病变患者的症状。在另一项试验中,181名患者被分为每天接受安慰剂或600、1200或1800mg α-硫辛酸组。1800mg/天组在短短一周内症状显著改善,600mg和1200mg组在第2周时症状有所改善1。在这两项试验中,疼痛和灼烧感都得到了缓解。另一项研究发现,在4年的时间里,每天口服600mg硫辛酸可以改善神经性症状,减缓轻度至中度糖尿病神经病变的进展8。
其他试验表明,静脉注射硫辛酸对糖尿病神经病变也有益。一项研究表明,每天静脉注射α-硫辛酸3周是治疗糖尿病神经病变的有效方法,另一项试验报告称,静脉注射2-4周是有效的1,9。
注意:硫辛酸有二种形式的补充剂:α-硫辛酸和R-硫辛酸。有证据表明,R-硫辛酸的钠盐比a-硫辛酸更具生物利用性10。
2.乙酰L肉碱(ALC)和L肉碱:
肉碱是一种对线粒体能量产生很重要的氨基酸类化合物。对肉碱在糖尿病神经病变中的作用源于有证据表明,患有并发症(包括糖尿病神经病变)的糖尿病患者的血清和总肉碱水平低于没有并发症的糖尿病患者11。因此,ALC和L-肉碱均已被研究为糖尿病神经病变的潜在治疗方法。补充肉碱可能有助于对抗肉碱缺乏症,改善胰岛素抵抗,使细胞更有效地利用葡萄糖,帮助受损神经纤维再生,或支持受损神经元更有效地运输细胞内成分11。
已经对补充肉碱对糖尿病神经病变的影响进行了多项人体试验。一项研究发现,L-肉碱(每天2g,持续10个月)可以改善神经传导速度,而神经传导速度在糖尿病神经病变中受损12。对ALC的研究发现,它减轻了糖尿病神经病变患者的疼痛,改善了腿部的振动感,并增加了神经再生13-15。补充肉碱也可能有助于治疗糖尿病引起的自主神经病变,对动物模型进行的一项研究发现ALC降低了糖尿病自主神经病变的心血管体征16。
3.十六酰胺乙醇(PEA):
一种天然存在于全身组织中的脂质化合物,包括中枢神经系统。在大豆卵磷脂、蛋黄和花生等食物中也存在17。越来越多的研究表明,补充PEA可能有效缓解各种原因引起的疼痛,而不会引发不良副作用18,19。大多数现有的临床前研究表明,PEA通过改变某些基因的表达和减少炎症信号传导发挥作用,但也提出了其镇痛作用的其他可能机制,包括其通过神经系统中的大麻素受体刺激信号传导的能力20,21。
几项临床试验表明,PEA可以减轻多种原因引起的疼痛,包括糖尿病神经病变、化疗诱导的周围神经病变、坐骨神经压迫、腕管综合征、骨关节炎、腰痛、背部手术失败、中风相关神经痛、多发性硬化症、牙痛、慢性骨盆疼痛、疱疹后神经痛和阴道疼痛等22。在一项针对因各种情况而无法通过常规治疗控制疼痛的慢性疼痛患者的观察性研究中,在三周内每天二次添加600mg PEA,然后在四周内每天一次,降低了所有完成研究的参与者的平均疼痛强度得分23。。
在一项随机对照试验中,636名因坐骨神经压迫而疼痛的参与者接受了每天300mg PEA、每天600mg PEA或安慰剂以及他们常用的止痛药,为期三周。两种剂量的PEA都比安慰剂更能减轻疼痛,而且高剂量比低剂量更有效。事实上,600mg组的疼痛评分降低了50%以上24。在118名神经疼痛患者中,30天的标准治疗加上每天600mg PEA比单独的标准治疗更有效25。一项随机临床试验发现,在缓解颞下颌关节(TMJ)疼痛方面,一周内每天900mg PEA,一周后每天600mg PEA比布洛芬更有效,布洛芬的剂量为600mg,两周内每天三次26。
对PEA的微粉化制剂也进行了研究。微粉化会产生更小的颗粒,这些颗粒可能更容易被吸收。剂量为600–1200mg/天的微粉化PEA可减轻糖尿病或创伤相关神经疼痛、背部手术失败后的慢性疼痛和拔牙后的急性疼痛受试者的疼痛27-29。在一份关于100例与脊柱疾病相关的神经疼痛的报告中,将超微粉化PEA补充剂纳入疼痛管理治疗显示出了有希望的结果30。一项荟萃分析发现,患有子宫内膜异位症引起的慢性盆腔疼痛的女性似乎受益于每天800mg微粉化PEA加上每天80mg虎杖苷(Polydatin)的组合,虎杖苷是一种在葡萄和红酒中发现的天然自由基减少剂31。在一项随机对照试验中,PEA和虎杖苷的组合在减轻肠易激综合征患者腹痛方面比安慰剂更有效32。
4. N-乙酰半胱氨酸(NAC):
既是体内谷胱甘肽合成前体,NAC本身也是一种抗氧化剂。它可以保护神经元免受氧化损伤33。此外,NAC已被证明可以抑制糖基化终产物(AGEs)的形成34。对糖尿病神经病变动物模型的多项研究发现,NAC可以防止神经元死亡并防止神经损伤33,2。
5.维生素B族:
B族维生素是一种维生素家族,在人体中发挥着许多作用,尤其是在细胞能量生成和神经系统功能中35。
5.1.维生素B1(硫胺素)和苯磷硫胺:
硫胺素缺乏可直接导致神经病变2。先前研究发现硫胺素可以用于治疗疼痛的糖尿病神经病变。苯磷硫胺是硫胺素的脂溶性衍生物,更容易被消化道吸收36。
苯磷硫胺可能调节导致糖尿病神经病变的几种途径:AGEs的形成、蛋白激酶C途径,以及由于高糖水平可能在细胞内发生的损伤性变化37,38。它也可能有助于预防导致神经病变的血管问题39。(Stracke 2008)多项临床试验已经检验了苯磷硫胺对糖尿病神经病变的影响39,40,2,并发现特别是在每天300至600mg的剂量下,它能够缓解糖尿病神经病变症状,尤其是疼痛。
5.2.维生素B12:它对神经系统的功能至关重要,缺乏B12会导致严重的周围神经病变2。此外,糖尿病神经病变患者通常具有高水平的破坏血管的化合物—同型半胱氨酸,在维生素B12水平较低的情况下,同型半胱氨酸会升高41。还研究了补充维生素B12治疗糖尿病神经病变的潜在益处,维生素B12的活性形式—甲钴胺,它对神经组织具有亲和力,在这方面已经得到了广泛的研究42。对糖尿病神经病变动物模型的研究发现,甲钴胺可以减轻糖尿病神经病变引起的损害,可能通过调节蛋白激酶C信号通路或激活化学信号来帮助神经存活和再生42,43。
在多项临床试验中发现,2mg甲钴胺、3mg L-甲基叶酸和35mg 5’-磷酸吡哆醛(维生素B6形式之一)的组合可以改善神经病变症状,并有助于维持下肢小神经的健康44-46。这三种营养素的组合也被发现有助于降低糖尿病神经病变患者的住院和医疗费用47。对甲钴胺的单独研究也令人鼓舞,口服甲基钴胺(每天1500mcg)和注射甲基钴胺(每天2000mcg)均可改善麻木、反射、对振动的敏感性、针刺刺激、步态和疼痛48,49。一项研究甚至发现,甲钴胺比常用于治疗糖尿病神经性疼痛的抗抑郁药去甲替林更有效48。
5.3.叶酸和维生素B6:与甲钴胺一样,维生素B6对神经功能很重要,而叶酸可能有助于改善供应神经的血管功能45。如前所述,叶酸和维生素B6衍生物以及甲钴胺已在临床试验中进行了测试,并显示出阳性结果44-46。
6. 维生素C和E:
研究发现,糖尿病患者的维生素C水平较低;这似乎是疾病本身的结果,而不是维生素C的饮食摄入减少50。另一项表明维生素C重要性的证据是,患有糖尿病神经病变的人体内“还原”的维生素C水平升高,而维生素C已经被人体使用。这表明糖尿病神经病变给身体储存的维生素C带来了额外的压力。研究表明,糖尿病神经病变患者和糖尿病动物的维生素E水平也有所下降51。已经发现,单独补充维生素E可以改善周围神经病变的症状52,还可以改善2型糖尿病患者的神经传导53。此外,包括维生素C和E等微量元素的治疗在一项临床试验中表明都是有益的54。
7.矿物质:
一项研究发现,糖尿病患者的头发和血液中锌、铬和锰含量较低,这表明这些营养素的缺乏可能与糖尿病神经病变有关55。此外,糖尿病是导致继发性镁缺乏的最常见疾病,25-30%的1型糖尿病患者和13.5-47.7%的2型糖尿病患者存在镁缺乏症56。在糖尿病大鼠模型中,口服镁或镁释放化合物有助于保护神经免受糖尿病神经病变的影响56,57。
一项临床试验还发现,连续5年每天口服500mg镁补充剂可以减缓人类糖尿病神经病变的进展58。锌也显示出治疗糖尿病神经病变的前景。临床研究发现,补充锌有助于改善血糖控制,还可以降低糖尿病神经病变的严重程度59,60。最后,一项临床研究发现,连续4个月补充微量营养素,包括锌和镁,以及维生素C和E,无论是否补充B组的维生素,都能改善糖尿病神经病变的症状54。
8.欧米伽-3脂肪酸:
历来被研究其对血管疾病的影响,因为高ω-3脂肪酸的饮食与较低的心脏病风险有关。虽然缺乏关于ω-3脂肪酸特别是在糖尿病神经病变中的益处的临床试验数据,但糖尿病神经病变的几种动物模型表明了这些重要脂肪的潜在作用61。一种理论认为,糖尿病神经病变与受影响神经膜中ω-3脂肪酸水平较低有关。对糖尿病神经病变动物模型的两项不同研究发现,补充ω-3脂肪酸可以改善糖尿病神经病变的症状62,63。
9.维生素D:
据报道,维生素D缺乏是糖尿病周围神经病变发展的独立风险因素64,补充维生素D可能有助一些患有神经病变的糖尿病患者。维生素D缺乏症同时存在于1型和2型糖尿病患者中,在有明显神经病变症状和疼痛阈值降低的糖尿病患者中更为常见65。一项针对患有糖尿病的成年人的研究报告称,维生素D不足(定义为水平低于30ng/mL)与更严重的自我报告的糖尿病神经病变症状有关,即使对几个变量进行了调整,如肥胖或糖尿病持续时间和控制,这种关联仍然存在66。
关于补充维生素D对糖尿病神经病变和维生素D缺乏症患者的影响,已经发表了两篇不同的论文。一项针对51名2型糖尿病患者的研究发现,补充维生素D可将报告的疼痛水平降低近50%,并表明维生素D可作为糖尿病神经病变引起的疼痛患者的“止痛药”67。第二个是一名维生素D缺乏症和糖尿病神经病变患者的病例报告,该患者严重到需要使用麻醉性止痛药来控制症状。该患者通过补充维生素D获得了显著的疼痛缓解,这表明服用维生素D可以显著缓解糖尿病神经病变症状65。
维生素D不足在各类人群中较为普遍,一般维持健康的血清25-羟基维生素D水平范围:50-80ng/mL。
10.植物化学素:
10.1.姜黄素:
姜黄素阿育吠陀医学的重要药草姜黄的主要活性成分。姜黄素具有抗氧化、抗炎特性。有证据表明,姜黄素可以通过降低氧化氮的自由基水平和抑制炎症介质TNF-α来调节疼痛感觉68。因此,它可能会干扰糖尿病神经病变损伤神经的疼痛信号,并防止对神经的氧化损伤69。
姜黄素用于糖尿病神经病变的主要证据来源于临床前研究。在糖尿病神经病变的动物模型中,已发现姜黄素可减少中枢和外周神经系统神经的氧化损伤,并减少了细胞死亡69,70。其他研究发现,姜黄素在这种疾病的动物模型中降低了炎症和对疼痛的敏感性71-73。
10.2.白藜芦醇和葡萄籽提取物:
白藜芦醇是一种天然的植物化学物质,存在于葡萄、红酒和日本虎杖中。在糖尿病动物模型中,白藜芦醇由于其抑制炎症以及减少氧化应激和DNA损伤的能力而被证明可以预防神经病变74,75。在另一项临床前研究中,发现白藜芦醇与胰岛素联合使用可降低对疼痛的敏感性71。
葡萄籽原花青素在糖尿病动物模型中被证明可以提高运动神经的传导速度并调节疼痛感;它们还减少了神经周围被称为髓鞘的保护鞘的损失。此外,它们减少了AGEs的产生,这表明它们还减少了糖尿病神经病变对神经的氧化损伤76
更多内容可点击其个性化综合干预方案如下:
- 自主神经病变防控(内脏等)
- 外周神经病变防控(肢端等)
- 周围神经病变防控(脑、眼等)
- 单神经病变防控
- 防止臀腿肌萎缩
- 糖尿病末梢神经炎防控
- 糖尿病性功能障碍(40-50岁)
- 糖尿病性功能障碍(51-60岁)
- 糖尿病性功能障碍(61-70岁)
- 糖尿病性功能障碍(71岁以上)
以及参阅本如下专文的相关内容:
医疗干预
医学上,仍然没有针对糖尿病神经病变的预防治疗措施,只能对症治疗。
取决于病程发展的症状。药物可用于缓解疼痛、灼烧感、刺痛或麻木等。治疗这些症状的药物与用于治疗癫痫发作和抑郁症的基本相同。
治疗疼痛的另一个选择称为经皮神经电刺激(TENS),将无痛的电信号通过皮肤发送到神经。医生可能会提供这种治疗。
手术治疗:(略)
自我护理
足部护理:对于糖尿病神经病变,需要特别关注脚部健康,因为足部神经是最常受神经病变影响的神经。脚部护理包括定期拜访医生,仔细检查、清洁和处理伤口等。此外,一定要穿合脚的鞋子,注意腿脚保暖,维持血液循环。
预防
预防糖尿病神经病变的最好方法是定期监测和管理好血糖水平,同时注意加强优质营养、防止营养缺乏症等。参考文献:
1. McIlduff CE et al. Critical Appraisal of the Use of Alpha Lipoic Acid (Thiooctic Acid) in the Treatment of Symptomatic Diabetic Polyneuropathy. Therapeutics and Clinical Risk Management, 2011; 7: 377-385.
2. Head KA. Peripheral Neuropathy: Pathogenic Mechanisms and Alternative Therapies. Alternative Medicine Review, 2006; 11(4): 294-329.
3. Korotchkina LG et al. R-lipoic acid inhibits mammalian pyruvate dehydrogenase kinase. Free radical research. Oct 2004;38(10):1083-1092.
4. Thirunavukkarasu V et al. Lipoic acid improves glucose utilisation and prevents protein glycation and AGE formation. Die Pharmazie. Oct 2005;60(10):772-775.
5. Kunt T et al. Alpha-lipoic acid reduces expression of vascular cell adhesion molecule-1 and endothelial adhesion of human monocytes after stimulation with advanced glycation end products. Clinical science. Jan 1999;96(1):75-82.
6. Bharat S et al. Pre-treatment with R-lipoic acid alleviates the effects of GSH depletion in PC12 cells: implications for Parkinson's disease therapy. Neurotoxicology. Oct 2002;23(4-5):479-486.
7. Bertolotto F et al. Combination of Alpha Lipoic Acid and Superoxide Dismutase Leads to Physiological and Symptomatic Improvements in Diabetic Neuropathy. Drugs Research and Development, 2012; 12(1): 29-34.
8. Ziegler D et al. Efficacy and Safety of Antioxidant Treatment with Alpha-Lipoic Acid Over 4 Years in Diabetic Polyneuropathy. Diabetes Care, 2011; 34: 2054-2060.
9. Han T et al. A Systematic Review and Meta-Analysis of Alpha-Lipoic Acid in the Treatment of Diabetic Peripheral Neuropathy. European Journal of Endocrinology, 2012; 167: 465-471.
10. Carlson DA et al. The plasma pharmacokinetics of R-(+)-lipoic acid administered as sodium R-(+)-lipoate to healthy human subjects. Alternative medicine review. Dec 2007;12(4):343-351.
11. Evans JD et al. Role of Acetyl-L-Carnitine in the Treatment of Diabetic Peripheral Neuropathy. Annals of Pharmacotherapy, 2008; 42: 1686-1691.
12. Ulvi H et al. Effect of L_Carnitine on Diabetic Neuropathy and Ventricular Dispersion in Patients with Diabetes Mellitus. Turkish Journal of Medical Science, 2010; 40(2): 169-175.
13. Bansal V et al. Diabetic Neuropathy. Postgraduate Medical Journal, 2006; 82: 95-100.
14. Sima AAF et al. Acetyl-L-Carnitine Improves Pain, Nerve Regeneration, and Vibratory Perception in Patients with Chronic Diabetic Neuropathy. Diabetes Care, 2005; 28(1): 89-94.
15. Adriaensen H et al. Critical Review of Oral Drug Treatments for Diabetic Neuropathic Pain – Clinical Outcomes Based on Efficacy and Safety Data from Placebo-Controlled and Direct Comparative Studies. Diabetes/Metabolism Research and Reviews, 2005; 21: 231-240.
16. Giudice PL et al. Autonomic Neuropathy in Streptozotocin Diabetic Rats: Effect of Acetyl-L-Carnitine. Diabetes Research and Clinical Practice, 2002; 56: 173-180.
17. Mattace Raso G et al. Palmitoylethanolamide in CNS health and disease. Pharmacological Research. Aug 2014;86:32-41.
18. Artukoglu BB et al. Efficacy of Palmitoylethanolamide for Pain: A Meta-Analysis. Pain Physician. Jul 2017;20(5):353-362.
19. Paladini A et al. Palmitoylethanolamide, a Special Food for Medical Purposes, in the Treatment of Chronic Pain: A Pooled Data Meta-analysis. Pain Physician. Feb 2016;19(2):11-24.
20. Gabrielsson L et al. Palmitoylethanolamide for the treatment of pain: pharmacokinetics, safety and efficacy. British Journal of Clinical Pharmacology. Oct 2016;82(4):932-942.
21. Khasabova IA et al. Peroxisome proliferator-activated receptor alpha mediates acute effects of palmitoylethanolamide on sensory neurons. The Journal of Neuroscience. Sep 12 2012;32(37):12735-12743.
22. Keppel Hesselink JM et al. Therapeutic utility of palmitoylethanolamide in the treatment of neuropathic pain associated with various pathological conditions: a case series. Journal of Pain Research. 2012;5:437-442.
23. Gatti A et al. Palmitoylethanolamide in the treatment of chronic pain caused by different etiopathogenesis. Pain Medicine (Malden, Mass.). Sep 2012;13(9):1121-1130.
24. Keppel Hesselink JM et al. Palmitoylethanolamide, a neutraceutical, in nerve compression syndromes: efficacy and safety in sciatic pain and carpal tunnel syndrome. Journal of Pain Research. 2015;8:729-734.
25. Dominguez CM et al. N-palmitoylethanolamide in the treatment of neuropathic pain associated with lumbosciatica. Pain Management. Mar 2012;2(2):119-124.
26. Marini I et al. Palmitoylethanolamide versus a nonsteroidal anti-inflammatory drug in the treatment of temporomandibular joint inflammatory pain. Journal of Orofacial Pain. Spring 2012;26(2):99-104.
27. Cocito D et al. Short-term efficacy of ultramicronized palmitoylethanolamide in peripheral neuropathic pain. Pain Research and Treatment. 2014;2014:854560.
28. Paladini A et al. Palmitoylethanolamide in the Treatment of Failed Back Surgery Syndrome. Pain Research and Treatment. 2017;2017:1486010.
29. Bacci C et al. Randomized split-mouth study on postoperative effects of palmitoylethanolamide for impacted lower third molar surgery. ISRN Surgery. 2011;2011:917350.
30. Chirchiglia D et al. Nonsurgical lumbar radiculopathies treated with ultramicronized palmitoylethanolamide (umPEA): A series of 100 cases. Neurol Neurochir Pol. 2018 Jan-Feb;52(1):44-47.
31. Indraccolo U et al. Micronized palmitoylethanolamide/trans-polydatin treatment of endometriosis-related pain: a meta-analysis. Annali Dell'Istituto Superiore di Sanita. Apr-Jun 2017;53(2):125-134.
32. Cremon C et al. Randomised clinical trial: the analgesic properties of dietary supplementation with palmitoylethanolamide and polydatin in irritable bowel syndrome. Alimentary Pharmacology & Therapeutics. Apr 2017;45(7):909-922.
33. Kamboj SS et al. N-Acetylcysteine Inhibits Hyperglycemia-Induced Oxidative Stress and Apoptosis Markers in Diabetic Neuropathy. Journal of Neurochemistry, 2010; 112: 77-91.
34. Nakayama M et al. Suppression of N(epsilon)-(carboxymethyl)lysine generation by the antioxidant N-acetylcysteine. Peritoneal dialysis international. May-Jun 1999;19(3):207-210.
35. Selhub J et al. B vitamins, homocysteine, and neurocognitive function in the elderly. The American journal of clinical nutrition. Feb 2000;71(2):614s-620s.
36. Sanchez-Ramirez GM et al. Benfotiamine Relieves Inflammatory and Neuropathic Pain in rats. European Journal of Pharmacology, 2006; 530: 48-53.
37. Varkonyi T et al. Diabetic Neuropathy: New Strategies for Treatment. Diabetes, Obesity and Metabolism, 2008; 10: 99-108.
38. Balakumar P et al. The Multifaceted Therapeutic Potential of Benfotiamine. Pharmacological Research, 2010; 61: 482-488.
39. Stracke H et al. Benfotiamine in Diabetic Polyneuropathy (BENDIP): Results of a Randomised, Double Blind, Placebo-Controlled Clinical Study. Exp Clin Endocrinol Diabetes. 2008 Nov;116(10):600-5.
40. Haupt E et al. Benfotamine in the treatment of diabetic polyneuropathy—a three-week randomized, controlled pilot study (BEDIP study). Int J Clin Pharmacol Ther. 2005;43(2):71-77.
41. Fahmy E et al. Estimation of Serum Homocysteine Level in Patients with Type 2 Diabetic Neuropathy. Egyptian Journal of Neurology Psychiatry and Neurosurgery, 2010; 47(1): 59-66.
42. Mizukami H et al. Methylcobalamin Effects of Diabetic Neuropathy and Nerve Protein Kinase C in Rats. European Journal of Clinical Investigation, 2011; 41(4): 442-450.
43. Okada K et al. Methylcobalamin Increases Erk1/2 and Akt Activities through the Methylation Cycle and Promotes Nerve Regeneration in a Rat Sciatic Nerve Injury Model. Experimental Neurology, 2010;222: 191-203.
44. Jacobs AM et al. Management of Diabetic Small-Fiber neuropathy with Combination L-Methylfolate, Methylcobalamin, and Pyridocal 5’-Phosphate. Reviews of Neurological Diseases, 2011; 8(1/2): 1-9.
45. Fonseca VA et al. Metanx in Type 2 Diabetes with Peripheral Neuropathy: A Randomized Trial. The American Journal of Medicine (2013) 126, 141-149.
46. Walker MJ et al. Improvement of Cutaneous Sensitivity in Diabetic Peripheral Neuropathy with Combination L-Methylfolate, Methylcobalamin, and Pyridoxal 5’Phosphate. Reviews in Neurological Diseases, 2010; 7(4): 132-139.
47. Wade RL et al. Impact of L-Methylfolate Combination therapy Among Diabetic Peripheral Neuropathy Patients. American Journal of Pharmacological Benefits, 2012; 4(5): 218-225.
48. Talaei A et al. Vitamin B12 may be more effective than nortriptyline in improving painful diabetic neuropathy. International Journal of Food Sciences and Nutrition, 2009;60 Suppl 5:71-6.
49. Dominguez JC et al. A prospective, open label, 24-week trial of methylcobalamin in the treatment of diabetic polyneuropathy. Journal of Diabetes Mellitus, 2012; 2(4): 408-412.
50. Sinclair AJ et al. Low Plasma Ascorbate Levels in Patients with Type 2 Diabetes Mellitus Consuming Adequate Dietary Vitamin C. Diabetic Medicine, 1994; 11(9): 893-898.
51. Ziegler D et al. Oxidative Stress and Antioxidant Defense in Relation to the Severity of Diabetic Polyneuropathy and Cardiovascular Autonomic Neuropathy. Diabetes Care, 2004; 27: 2178-2183.
52. Martinello F et al. Supplemental therapy in isolated vitamin E deficiency improves the peripheral neuropathy and prevents the progression of ataxia. Journal of Neurological Sciences 156 (1998) 177–179.
53. Tutuncu NB et al. Reversal of defective nerve conduction with vitamin E supplementation in type 2 diabetes: a preliminary study. Diabetes Care. 1998 Nov;21(11):1915-8.
54. Farvid MS et al. Improving neuropathy scores in type 2 diabetic patients using micronutrients supplementation. Diabetes Research and Clinical Practice, 2011; 93: 86-94.
55. Gul Kazi T et al. Copper, Chromium, Manganese, Iron, Nickel, and Zinc Levels in Biological Samples of Diabetes Mellitus Patients. Biol Trace Elem Res (2008) 122:1–18
56. Rondon LJ et al. Magnesium attenuates chronic hypersensitivity and spinal cord NMDA receptor phosphorylation in a rat model of diabetic neuropathic pain. Journal of Physiology, 2010; 588(21): 4205-4215.
57. Hosseini A et al. Benefit of magnesium-25 carrying porphyrinfullerenenanoparticles in experimental diabetic neuropathy. International Journal of Nanomedicine 2010:5 517–523.
58. De Leeuw I et al. Long term magnesium supplementation influences favourably the natural evolution of neuropathy in Mg-depleted type 1 diabetic patients (T1dm). Magnesium Research. 2004;17(2):109-114.
59. Jayawardena R et al. Effects of zinc supplementation on diabetes mellitus: a systematic review and meta-analysis. Diabetology & Metabolic Syndrome 2012, 4:13
60. Hayee MA et al. Diabetic Neuropathy and Zinc Therapy. Bangladesh Medical Reseanch Council Bull, 2005; 31(2): 62-67.
61. De Caterina R et al. n-3 Fatty Acids in the Treatment of Diabetic Patients. Diabetes Care, 2007l 30(4): 1012-1026.
62. Gerbi A et al. Fish Oil Supplementation Prevents Diabetes-Induced Nerve Conduction Velocity and Neuroanatomical Changes in Rats. The Journal of Nutrition, 1999; 129: 207-213.
63. Coste TC et al. Neuroprotective Effect of Docosahexaenoic Acid–Enriched Phospholipids in Experimental Diabetic Neuropathy. Diabetes, 2003; 52: 2578-2585.
64. Shehab D et al. Does Vitamin D deficiency play a role in peripheral neuropathy in Type 2 diabetes? Diabetic Medicine, 2012;29(1):43-9.
65. Bell DSH. Reversal of the Symptoms of Diabetic Neuropathy through Correction of Vitamin D Deficiency in a Type 1 Diabetic Patient. Case Rep Endocrinol. 2012;2012:165056.
66. Soderstrom LH et al. Association between vitamin D and diabetic neuropathy in a nationally representative sample: results from 2001-2004 NHANES. Diabetic Medicine, 2012;29(1):50-5.
67. Lee P et al. Vitamin D as an Analgesic for Patients With Type 2 Diabetes and Neuropathic Pain. Archives of Internal Medicine, 2008; 168(7): 771-772.
68. Sharma S et al. Curcumin attenuates thermal hyperalgesia in a diabetic mouse model of neuropathic pain. European Journal of Pharmacology, 2006; 536: 256-261.
69. Lakshmanan AP et al. Curcumin attenuates hyperglycaemia-mediated AMPK activation and oxidative stress in cerebrum of streptozotocin-induced diabetic rat. Free Radical Research, July 2011; 45(7): 788–795.
70. Acar A et al. Oxidative Damage is Ameliorated by Curcumin Treatment in Brain and Sciatic Nerve of Diabetic Rats. International Journal of Neuroscience, 2012; 122(7): 367-372.
71. Sharma S et al. Effect of Insulin and its Combination with Resveratrol or Curcumin in Attenuation of Diabetic Neuropathic Pain: Participation of Nitric Oxide and TNF-alpha. Phytotherapy Research, 2007; 21: 278-283.
72. Kulkarni SK et al. An Overview of Curcumin in Neurological Disorders. Indian J Pharm Sci. 2010 Mar-Apr; 72(2): 149–154.
73. Attia HN et al. Protective effects of combined therapy of gliclazide with curcumin in experimental diabetic neuropathy in rats. Behavioural Pharmacology, 2012; 23(2): 153-161.
74. Kumar A et al. Effects of resveratrol on nerve functions, oxidative stress and DNA fragmentation in experimental diabetic neuropathy. Life Sciences, 2007;80(13):1236-44.
75. Kumar A et al. NF-kappaB inhibitory action of resveratrol: a probable mechanism of neuroprotection in experimental diabetic neuropathy. Biochemical and Biophysical Research Communications 2010;394(2):360-5.
76. Cui XP et al. Effects of grape seed proanthocyanidin extracts on peripheral nerves in streptozocin-induced diabetic rats. Journal of Nutritional Science and Vitaminology (Tokyo), 2008;54(4):321-8.
参考来源:
美国糖尿病协会
http://www.diabetes.org
美国国立卫生研究院糖尿病、消化和肾病研究所
https://www.niddk.nih.gov
加拿大糖尿病协会
http://www.diabetes.ca
加拿大卫生部
http://www.hc-sc.gc.ca
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

